Pisałem niedawno o różnego rodzaju patogenach, czyli przyczynach naszych chorób. Jednym z nich są bakterie. One właśnie były do niedawna jedną z głównych przyczyn śmierci: od zakażenia ran, do zapalenia płuc, bakterie odpowiadały za całą masę zgonów, których dziś możemy1Jeszcze! stosunkowo łatwo uniknąć. A wszystko dzięki przypadkowemu odkryciu pana Fleminga.
Alexander Fleming – odkrywca penicyliny
Alexander Fleming, bo o nim mowa2Nie miał nic wspólnego z Ianem Flemingiem, autorem książek o Jamesie Bondzie był szkockim lekarzem, który w czasie pierwszej wojny światowej służył w brytyjskiej armii. Miał tam możliwość naocznie przekonać się, jak wielu żołnierzy ginęło nie wprost od ran poniesionych na polu bitwy, ale od wtórnych zakażeń. Już wtedy był zainteresowany bakteriologią, ale to właśnie frontowe doświadczenia mogły go skłonić do późniejszego poświęcenia się pracy naukowej w tej dziedzinie.

Zajmował się więc badaniami nad różnymi szczepami bakterii. Konkretniej w roku 1928 badał bakterie gronkowca – czyli bakterie rodzaju Staphylococcus. A żeby bakterie badać, trzeba je wyhodować. Robi się to na szalkach Petriego, czyli na płaskich talerzach z pionową ścianką.
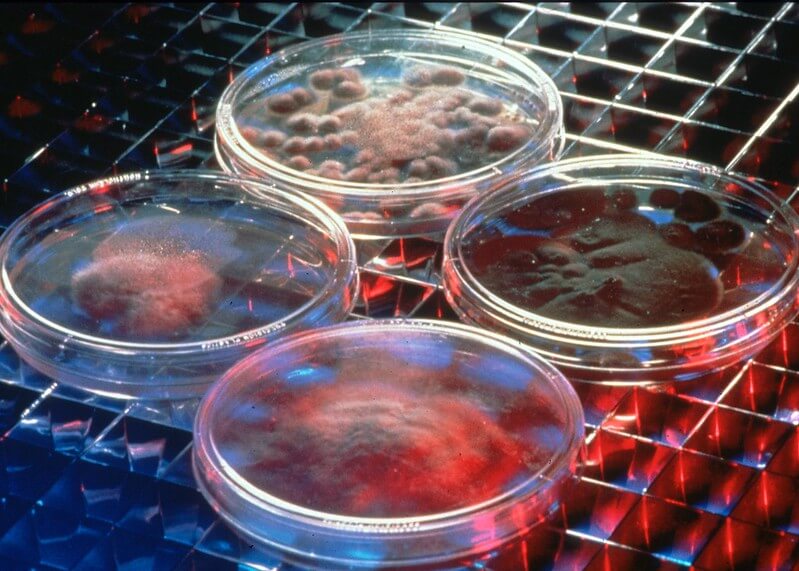
Do solidnych badań takich szalek trzeba niekiedy przygotować dosyć dużo. Tym bardziej, że w latach dwudziestych poprzedniego wieku dostępna aparatura badawcza była o wiele mniej czuła, niż dzisiaj. Ale wiele bakterii nie wymaga zbyt dużego dozoru, a naukowiec też człowiek3Przynajmniej w założeniu. i czasem potrzebuje urlopu. I tutaj Fleming też nie był wyjątkiem: żeby uniknąć długiego przestoju, w lipcu 1928 przygotował szalki z różnego rodzaju bakteriami gronkowca, po czym wyjechał na urlop. Gdy wrócił we wrześniu, zabrał się za przeglądanie szalek i… zauważył coś ciekawego.
Właściwości bakteriobójcze grzyba
Otóż na jednej z szalek wyrosła pleśń. Ot, zdarza się. W powietrzu unosi się bez liku różnego rodzaju mikroorganizmów; jeśli ktoś nie zachowa pewnych podstawowych zasad sterylnej pracy w laboratorium mikrobiologicznym, szybko się o tym przekona. Co więc było niezwykłego w tej pleśni? Otóż Fleming, szykując się już do wyrzucenia “zmarnowanej” szalki zauważył, że pomiędzy pleśnią a najbliższymi bakteriami istnieje pas “ziemi niczyjej”. Samo to, że w miejscu, w którym rósł grzyb, nie rosły bakterie, nie jest niczym niezwykłym. Ot, pleśń była lepiej przystosowana, zajęła miejsce, efektywnie zagospodarowała zasoby, dla bakterii nic już nie zostało. Ale ta pleśń dała radę utrzymać bakterie w pewnej odległości od siebie! To oznacza, że musiała wydzielać coś, co bakterie zwalcza!

Okazało się więc, że ludzka intuicja w tym temacie była już wcześniej wyjątkowo poprawna. Pamiętacie może, jak w ”Ogniem i mieczem” Zagłoba polecił zagnieść pajęczyny z chlebem dla rannego Bohuna? Wprawdzie badania wykazały, że sama pajęczyna nie ma właściwości bakteriobójczych, ale jak się okazuje, na pajęczynie często można znaleźć grzyby tego samego rodzaju, co te znalezione przez Fleminga. W połączeniu z wilgotnym chlebem mogły się one rozwijać, produkując swój środek do walki z bakteriami.
Mówimy tu o grzybach rodzaju Penicillium, od których nazwano tez związek odkryty przez Fleminga – penicylinę. Do czego jest ona grzybom potrzebna? Cóż, do prowadzenia wojny. Trzeba pamiętać, że wojny między ludźmi są niczym w porównaniu do wojny, którą toczą między sobą mikroorganizmy. Jest to nieustająca wojna o przetrwanie, w której wszystkie chwyty są dozwolone. A penicylina, którą grzyby produkują, gdy coś im przeszkadza w powiększaniu kolonii, jest bronią chemiczną wykorzystywaną na tej wojnie.
Jak działa penicylina?
Przede wszystkim, trzeba wiedzieć, że bakterie posiadają ścianę komórkową. W jej skład wchodzi coś w rodzaju “włókien”4Fachowo nazywa się to peptydoglikan. Włókna te mają wypustki, którymi łączą się z innymi włóknami, tworząc tym samym gęstą sieć, utrzymująca zawartość komórki bakterii tam, gdzie być powinna. Penicylina podobna jest do końcówek tych wypustek:
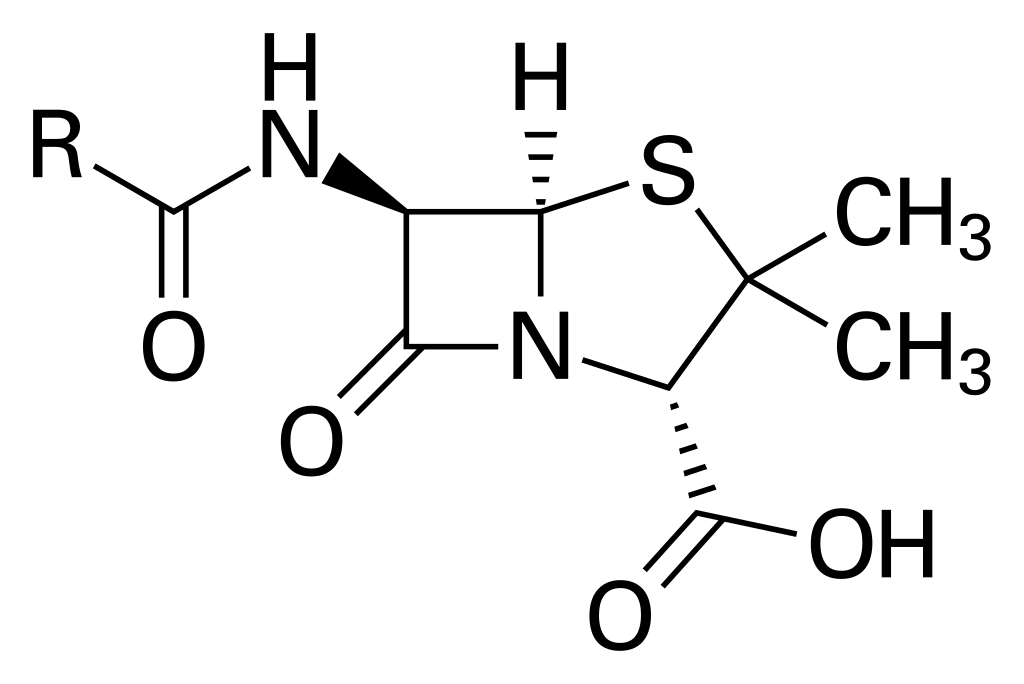
Jeśli spojrzycie na strukturę penicyliny przedstawioną powyżej, może Wam się rzucić w oczy ulokowany centralnie kwadrat. Te kreski obrazują wiązania chemiczne, zaś w rogach kwadratu znajduje się atom azotu (N) oraz trzy atomy węgla. Te atomy bardzo chciałyby tworzyć wiązania pod kątem około 110 stopni. Jednak kwadrat oznacza, że kąt pomiędzy wiązaniami wynosi 90 stopni. Co to oznacza? To samo, co by się stało, gdybyście solidnie wygięli prostą gałąź: pojawi się na niej duże naprężenie. Gałąź zgromadzi dużo energii, którą chętnie odda przy najbliższej okazji.
I nie inaczej jest z naszą penicyliną. Ponieważ jest podobna do końcówek “wypustek”, jest rozpoznawana przez enzym, który łączy ze sobą poszczególne włókna ściany komórkowej. A gdy już penicylina dostanie się do środka enzymu, ten kwadratowy pierścień się otwiera i reaguje z enzymem. Sprawia to, że penicylina już go nie może opuścić, więc enzym nie może normalnie działać. Tym samym budowa ściany komórkowej zostaje zatrzymana. Ale komórka bakterii o tym “nie wie”, tylko dalej próbuje się podzielić… A gdy dzieli się, mając niesprawną ścianę komórkową, cała jej zawartość “wycieka” na zewnątrz i na tym jej życie się kończy.
Sok z pleśni
Fleming jednak o tym wszystkim nie wiedział. Podjął próbę oczyszczenia związku odpowiedzialnego za efekt bakteriobójczy, ale głównym rezultatem było stwierdzenie, że jest on nietrwały – łatwo ulega rozkładowi. Dziś wiemy, że za to również odpowiada ten silnie naprężony kwadrat, o którym pisałem wyżej. Tak czy inaczej, był co najwyżej w stanie uzyskać filatrat “soku z pleśni”, w którym znajdowała się penicylina.

Poza tym, badania wykonywane na różnych rodzajach bakterii wykazały, że niektóre ich rodzaje penicylina niszczy bardzo skutecznie, a na niektóre nie ma żadnego wpływu. Dlatego też początkowo Fleming myślał o wykorzystaniu nowej substancji do ułatwienia różnicowania bakterii. Otóż można by je stosunkowo łatwo dzielić na te wrażliwe i niewrażliwe na penicylinę. Natomiast to pozwoliłoby na łatwiejsze określenie, z jakim konkretnie gatunkiem mamy do czynienia. Widział nawet potencjał w zastosowaniu “soku z pleśni” jako dodatku do hodowli bakterii niewrażliwych na penicylinę, co miało zapobiec zanieczyszczeniu hodowli innymi rodzajami bakterii. I tylko mimochodem wspomniał o potencjale stosowania penicyliny w lecznictwie.
Pierwsze próby z antybiotykiem
Ale to właśnie ta możliwość miała mu zapewnić sławę. Już w 1930 roku udały się pierwsze próby leczenia bakteryjnych zakażeń oczu. Później Fleming prowadził więcej eksperymentów na pacjentach – choć trzeba zauważyć, że nie były one tak rygorystyczne jak te, które prowadzi się dziś. Jednak dopiero rok 1942 przyniósł prawdziwe przełomy. Po pierwsze, udało się wreszcie wyizolować – choć w niewielkiej ilości – czystą penicylinę. To pozwoliło na określenie jej struktury chemicznej5Ostatecznie potwierdzonej przez późniejszą noblistkę, Dorothy Hodgkin. A z drugiej strony, wysiłek włożony w zebranie materiału do tej izolacji, jak też do prób klinicznych, przekonał naukowców, że potrzebne jest opracowanie przemysłowej metody produkcji penicyliny. A trzy lata później Fleming, wraz z chemikami: Ernstem Chainem i Howardem Floreyem, podzielili się nagrodą Nobla z medycyny.
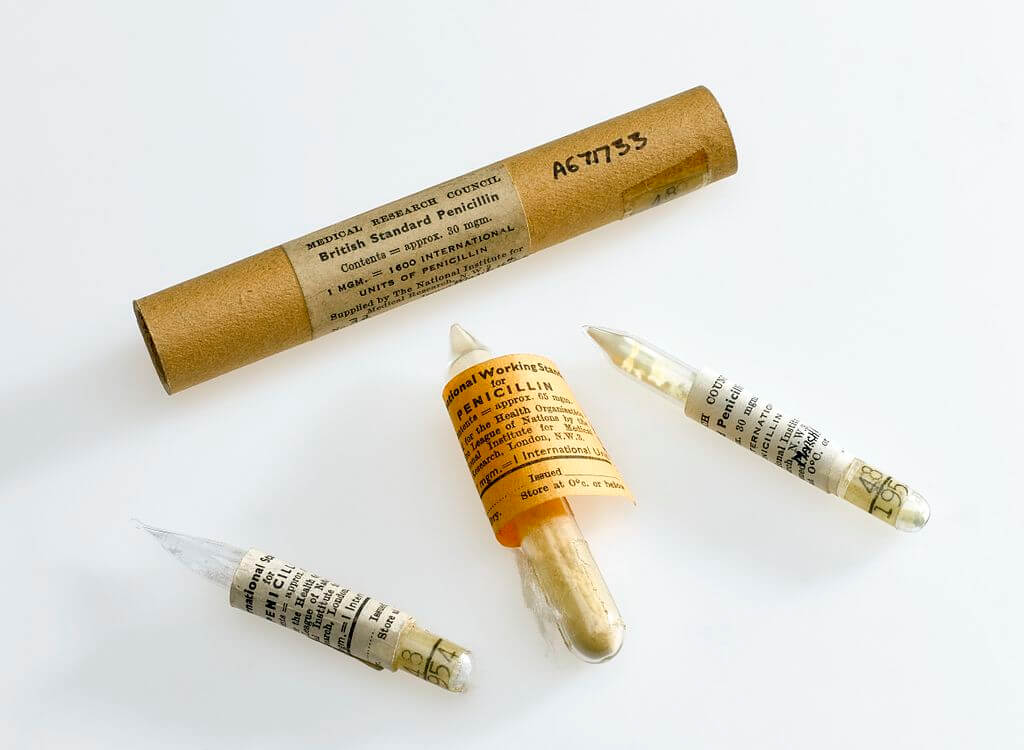
Odkrycie i wdrożenie tego pierwszego antybiotyku przyniosło rewolucję. Wiele ran i chorób nagle stało się uleczalne. W czasie drugiej wojny światowej Alianci wykorzystywali penicylinę do ratowania rannych żołnierzy, ale po wojnie szybko przyjęła się również w cywilnej medycynie. Niestety, okazało się, że bakterie z czasem mogą nabierać odporności na działalność tego antybiotyku6Antybiotykoodporność swoją drogą jest jednym z największych – i często niedocenianych – zagrożeń dla ludzkości, o czym szerzej napiszę przy innej okazji. I tak zaczął się nasz wyścig zbrojeń w wojnie przeciwko mikrobom.

Penicylina i przyjaciele
Przede wszystkim, zaczęto pracować nad uzyskaniem pochodnych penicyliny, czyli związków podobnych do niej, ale jednak różniących się nieco aktywnością czy możliwością “wymykania się” przed strategiami obronnymi bakterii. Te starania przyspieszyły po opracowaniu metody chemicznej syntezy penicyliny. Kolejne półsyntetyczne, a potem syntetyczne analogi miały coraz korzystniejsze dla człowieka właściwości. Opracowano między innymi bazujące na penicylinie antybiotyki, które są odporne na bakteryjne β-laktamazy, czyli enzymy rozkładające penicylinę. Opracowano też dodatek do antybiotyków penicylinowych, zwany kwasem klawulanowym.
Ten ze względu na swoją strukturę podszywa się pod penicylinę i unieczynnia β-laktamazy, pozwalając penicylinie zrobić swoje. A czy nazwa kwas klawulanowy się Wam z czymś kojarzy? Ci, którzy odpowiedzieli “amoksiklav” mogą sobie dodać punkt. Ten często stosowany antybiotyk bazuje właśnie na mieszaninie amoksycyliny, czyli pochodnej penicyliny, oraz kwasu klawulanowego. Stosowaliście go kiedyś na sobie lub swoich bliskich? Jeśli tak, to zawdzięczacie go między innymi przypadkowemu odkryciu Aleksandra Fleminga sprzed ponad dziewięćdziesięciu lat. Warto też zauważyć, że nawet “oryginalna” penicylina, dziś znana pod nazwą penicyliny G, wciąż znajduje zastosowanie w postaci zastrzyków dożylnych lub domięśniowych. A z drugiej strony, choć my staramy się rozwijać nowe metody walki z bakteriami, te nie pozostają w tyle. Skrót MRSA oznaczający gronkowca złocistego odpornego na metycylinę, potrafi spędzić sen z powiek lekarzom…
Jak wygląda przyszłość w naszej walce z mikroorganizmami? Nie mamy pewności. Dziś wiemy, że patogeny wciąż mutują, uzyskując odporność na nowe antybiotyki, a nam powoli kończą się pomysły na modyfikacje tych, które już istnieją. Czy uda nam się wymyślić nowy sposób walki z nimi? Są pewne przesłanki sugerujące, że tak, o tym jednak więcej napiszę innym razem. Na pewno wiadomo, że mało odkryć przyczyniło się do tylu uratowanych żyć, co to dokonane przypadkiem przez Aleksandra Fleminga.
Źródła:
https://www.acs.org/content/acs/en/education/whatischemistry/landmarks/flemingpenicillin.html
https://www.sciencedirect.com/science/article/pii/S2589004221010932
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2041430/
Zainteresowało Cię to, co czytasz? Chcesz wiedzieć więcej? Śledź nas na Facebooku, i – pozwól, że wyjaśnię!

[…] bakterie mogą w różny sposób radzić sobie z tymi antybiotykami. Czasem, jak choćby w wypadku penicyliny, wytwarzają enzymy, które są w stanie zniszczyć antybiotyk, zanim ten zadziała. Czasem po […]
[…] wojnie biologicznej już u nas mogliście przeczytać – choćby wtedy, gdy pisaliśmy o penicylinie. Dziś przenosimy się na nieco większą skalę: już nie mikroorganizmy, ale biedronki będą […]
[…] Ale to właśnie tzw. ciśnienie osmotyczne jest odpowiedzialne za śmierć bakterii potraktowanych penicyliną, która uniemożliwia im zbudowanie twardej ściany komórkowej i uniknięcie […]